Autoren: Frank R. Kloss, Peer W. Kämmerer und Anita Kloss-Brandstätter
Dieser Artikel erschien ursprünglich am 26. September 2023 auf Englisch im “Journal of Clinical Medicine 2023; 12(19), 6214 (published by MDPI)” unter dem Titel “First Clinical Case Report of a Xenograft–Allograft Combination for Alveolar Ridge Augmentation Using a Bovine Bone Substitute Material with Hyaluronate (Cerabone® Plus) Combined with Allogeneic Bone Granules (Maxgraft®)”.
https://doi.org/10.3390/jcm12196214
Die Originalpublikation ist ein Open Access Artikel unter den Bedingungen der Creative Commons Attribution License, die die Nutzung, Verbreitung und Vervielfältigung in jedem Medium erlaubt, sofern das Originalwerk ordnungsgemäß zitiert wird.
1. Hintergrund
Die Rekonstruktion der knöchernen Struktur des Kiefers mittels Alveolarkammaugmentation ist für eine erfolgreiche Implantatbehandlung von entscheidender Bedeutung. Allogene (von menschlichen Spendern) und xenogene (tierischen Ursprungs) Knochenersatzmaterialien sind neben anderen eine sichere und wirksame Option, um das Knochenvolumen aufzubauen, die Stabilität und Langlebigkeit von Dentalimplantaten sicherzustellen und die Entnahme von autologem Transplantat zu vermeiden 1,2,3. Die Fortschritte in der Medizintechnik haben zu bemerkenswerten Entwicklungen auf dem Gebiet der Knochenaugmentation geführt und verbesserte Ergebnisse nach verschiedenen oralchirurgischen Verfahren ermöglicht4,5,6,7,8. Eine dieser bahnbrechenden Entwicklungen ist cerabone® plus, ein vielversprechendes Knochenersatzmaterial, das sich bei der Alveolarkammaugmentation prae implantionem durch exzellente Handhabungseigenschaften auszeichnet. cerabone® plus ist ein Gemisch aus dem bovinen Knochenersatzmaterial cerabone® und Natriumhyaluronat (dem wasserlöslichen Salz der Hyaluronsäure). Bei Kontakt mit Kochsalzlösung oder Blut bildet es ein „Sticky-Bone“-Knochenersatzmaterial, das hervorragenden Anwendungskomfort bietet, da es sowohl die Aufnahme des Materials als auch die Applikation in den Defektbereich vereinfacht.
1.1. Bovine Knochenersatzmaterialien
Zahlreiche Studien belegen die Wirksamkeit des bovinen Knochenersatzmaterials cerabone® und haben aufgezeigt, dass cerabone® ein geeignetes Material für die Rekonstruktion des Alveolarkamms prae implantionem ist 7,9,10,11,12,13,14,15. Die ausgezeichnete Hydrophilie von cerabone® wurde in Hochgeschwindigkeits-Videomikroskopie-Analysen nachgewiesen 16. Im Einklang damit ergab eine Analyse der Regenerationskapazität und Immunantwort bei der Anwendung von xenogenen und synthetischen Knochenersatzmaterialien, dass das xenogene cerabone® eine stärkere antiinflammatorische Reaktion induzierte17,18,19. Übereinstimmend kam eine histologische, histomorphometrische und röntgenologische Analyse von cerabone® bei der Anwendung im Rahmen einer Sinusbodenelevation zu dem Ergebnis, dass dieses bovine Knochenersatzmaterial über exzellente osteokonduktive Eigenschaften und ein langsames Resorptionsprofil verfügt 20.
1.2. Biofunktionalisierung von Knochenersatzmaterialien
Da bereits nachgewiesen wurde, dass cerabone® vorteilhafte Eigenschaften für die orale Knochenregeneration besitzt, stellt sich die Frage, warum eine weitere Biofunktionalisierung erforderlich ist. Eine Untersuchung von verschiedenen Hydroxylapatit-haltigen Biomaterialien (einschliesslich cerabone®, Bio-Oss® und maxresorb®) für die Alveolarkammaugmentation in einem Tiermodell ergab, dass keines der untersuchten Hydroxylapatit-haltigen Biomaterialien die ortsständige Neubildung oder Maturation von Knochengewebe über die natürliche Regenerationskapazität dieses Tiermodells hinaus begünstigte. Dies deutet auf die Grenzen dieser Biomaterialien als eine regenerative Lösung hin21. Um die knöcherne Heilung und damit die Osseointegration und Stabilität von Dentalimplantaten zu verbessern, wurde cerabone® mit plättchenreichem Fibrin (PRF) vermischt. Tatsächlich enthielt diese Kombination aus natürlichem bovinen Hydroxylapatit (cerabone®) und PRF zusätzliche Wachstumsfaktoren, welche den Wundheilungsprozess und die Langzeitvolumenstabilität begünstigten22. Um Thrombozytenkonzentrate wie PRF herzustellen, ist aber leider eine Blutentnahme erforderlich. Daraus ergab sich die Überlegung, ob eine Biofunktionalisierung auch mithilfe von Hyaluronsäure anstelle von PRF erreicht werden könnte23,24.
Hyaluronsäure kommt als ein natürlicher Bestandteil in den menschlichen Körpergeweben und Organen vor und spielt bei zahlreichen physiologischen Prozessen eine wichtige Rolle. Beispielsweise unterstützt Hyaluronsäure die Zellwanderung und die Wundheilung und ist für den Feuchtigkeitsgehalt der Gewebe verantwortlich. In einer neueren Studie wurden optimierte bioaktive Polymere für die Knochenregeneration, darunter auch Hyaluronsäure, umfassend untersucht25. Da es sich bei Hyaluronsäure um ein natürlich vorkommendes, nicht toxisches, nicht inflammatorisches, biologisch abbaubares und biokompatibles Polymer handelt, sind bereits zahlreiche Medizinprodukte entwickelt worden, welche Hyaluronsäure enthalten. Bezogen auf eine verbesserte Osteogenese und Mineralisierung führten auf Hyaluronsäure basierende Komposit-Gerüste ebenfalls zu vielversprechenden Ergebnissen26. Eine verbesserte Osteogenese und Osseointegration kann mit Hyaluronsäure-basierten Mikropartikeln erreicht werden, welche kovalent an Implantatoberflächen aus Metall anhaften und bioaktive Komponenten freisetzen25. Der Vorteil der Biofunktionalisierung von Hydroxylapatiten mit Hyaluronsäure liegt darin, dass Hyaluronsäure aus hydrophilen Molekülen besteht, deren Salz (Natriumhyaluronat) auf einfache Weise durch die Zugabe von Kochsalzlösung aktiviert werden kann, womit die Notwendigkeit einer Blutentnahme entfällt.
In-vitro-Studien haben gezeigt, dass die Biofunktionalisierung des bovinen Knochenersatzmaterials cerabone® mit Hyaluronsäure im Menschen eine erhöhte Osteoblastenaktivität induziert. Dies deutet darauf hin, dass auf diese Weise eine verbesserte und beschleunigte Knochenregeneration erreicht werden kann24,27. Basierend auf den Ergebnissen der In-vitro-Studien wurde das innovative Knochenersatzmaterial in In-vivo-Modellen getestet. Die Wirksamkeit von Knochenersatzmaterialien für die maxillofaziale knöcherne Regeneration ist eng mit einer effizienten Induktion der Angiogenese korreliert. Die In-vivo-Angiogenese wurde signifikant stimuliert, wenn das xenogene Knochenersatzmaterial cerabone® mit Hyaluronsäure kombiniert wurde23. In weiteren Tiermodellen demonstrierte cerabone® plus eine ausgezeichnete Biokompatibilität und gute osteokonduktive Eigenschaften28,29. Zusätzlich wurde cerabone® plus erfolgreich im Rahmen von rekonstruktiven Periimplantitis-Therapien eingesetzt30 und in einem klinischen Fall für die Alveolarkammaugmentation31.
1.3. Klinische Anwendungen
2020 erhielt cerabone® plus die CE-Zertifizierung (https://botiss.com/de/botiss-entwickelt-innovatives-knochenersatzmaterial-mit-hyaluronsaeure/ (Stand 11. August 2023)). Dank der besonderen Eigenschaften von cerabone® plus wie Osteokonduktivität und Volumenstabilität ermöglicht dieses relativ neue bovine Knochenersatzmaterial eine effiziente und zeitsparende Defektfüllung sowie eine einfache Defektkonturierung 30,31. Nach der Hydratation ist cerabone® plus eine klebrige und formbare Masse, die eine präzise Applikation der Partikel ohne Verlagerung von einzelnen Granula ermöglicht24,27. Entsprechend ist cerabone® plus für horizontale und vertikale Augmentationsverfahren31, die Auffüllung von periimplantären Defekten30, Socket-Preservation-Verfahren und Sinuselevationen geeignet.
Dies ist der erste Fallbericht mit einem Nachbeobachtungszeitraum von drei Jahren, der die klinische Anwendung von cerabone® plus in Kombination mit allogenen Knochenpartikeln bei einer Alveolarkammaugmentation prae implantionem dokumentiert.
2. Materialien und Methoden
2.1. Zusammenfassung des klinischen Falls
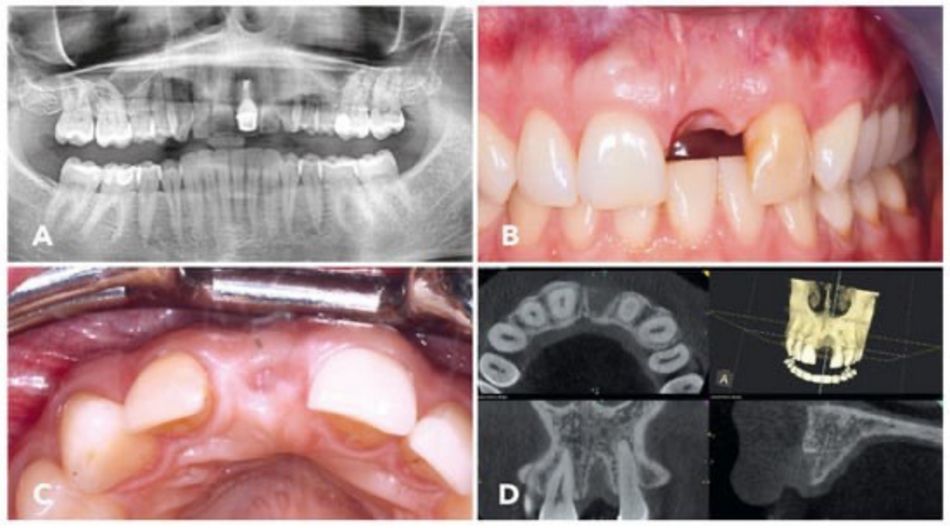
Dieser retrospektive klinische Fallbericht wurde gemäss der CARE-Leitlinie (Case Reporting (CARE) Guideline) erstellt32,33. Eine 34 Jahre alte Patientin stellte sich mit dem Wunsch nach einem festsitzenden Zahnersatz in Regio 21 vor. Infolge eines 15 Jahre zurückliegenden Traumas hatte sich der mittlere Schneidezahn im linken Oberkiefer gelockert. Die Patientin hatte sich bereits zwei Mal einer Wurzelresektion unterzogen. Auf der präoperativen Panorama-Röntgenaufnahme in Abbildung 1A ist eine periradikuläre Läsion an Zahn 21 zu erkennen. Bei der klinischen Untersuchung wurde eine bukkale Fistel festgestellt. Daher wurde entschieden, den Zahn zu extrahieren. Abbildung 1B zeigt die klinische Situation vier Monate nach der Extraktion von Zahn 21 mit teilweisem Verlust der distalen Papille. Die bukkale Knochenlamelle von Zahnfach 21 war atrophisch. Das Weichgewebe war gesund und entzündungsfrei. Eine breite Zone keratinisierter Gingiva war vorhanden. Abbildung 1C zeigt die klinische Situation in der palatinalen Ansicht. Zu erkennen ist ein geringfügiger Abbau des bukkalen Knochens, jedoch keine Entzündungszeichen.
Unmittelbar vor dem chirurgischen Augmentationsverfahren wurde eine präoperative DVT-Aufnahme angefertigt (Abbildung 1D). Die DVT-Aufnahme des Alveolarkamms zeigte einen transversalen Knochendefekt mit einer Restkammbreite von 2 bis 3 mm; dies entspricht einem Defekt der Klasse II nach Chen und Buser34 bzw. einem Klasse-4-Defekt (horizontaler Kammdefekt, der eine Knochenaugmentation prae implantionem erfordert) nach Benic und Hämmerle35. Gemäss den ITI-Empfehlungen zur Rekonstruktion von knöchernen Defekten wurde ein zweistufiges GBR-Verfahren (gesteuerte Knochenregeneration) geplant. Die Einstufung der restaurativen und chirurgischen Behandlungssituation der Patientin gemäss SAC-Klassifikation nach Dawson und Chen 36 ist in Tabelle 1 dargestellt. Die Patientin war gesund und es lagen keine Zeichen für eine Parodontalerkrankung vor. Die Patientin nahm keine regelmässigen Medikamente ein.
Tabelle 1. SAC-Klassifikation der Patientin.
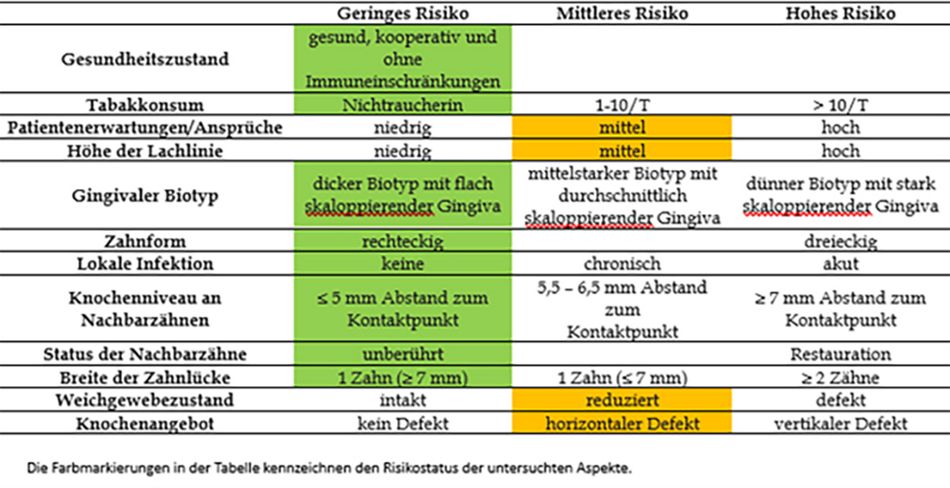
Die Farbmarkierungen in der Tabelle kennzeichnen den Risikostatus der untersuchten Aspekte.
Der Knochendefekt wurde mit einem Gemisch aus cerabone® plus (botiss biomaterials GmbH, Zossen, Deutschland), einer rein bovinen Knochenmineralkomponente mit Natriumhyaluronat, und allogenen Knochenpartikeln (maxgraft® Granula, botiss biomaterials GmbH, Zossen, Deutschland) rekonstruiert. Sechs Monate nach dem Augmentationsverfahren wurde ein Titanimplantat gesetzt. Die letzte Kontrollaufnahme wurde im Juni 2023 angefertigt. Insgesamt wurde die Patientin über einen Zeitraum von etwa 3 Jahren nach dem Augmentationsverfahren nachbeobachtet. Das chirurgische Verfahren wurde unter Lokalanästhesie in unserer Praxis in Lienz, Österreich, durchgeführt.
2.2. cerabone® plus
cerabone® plus (botiss biomaterials GmbH, Zossen, Deutschland) ist eine Kombination aus dem etablierten bovinen Knochenersatzmaterial cerabone® und Natriumhyaluronat, dem wasserlöslichen Salz der Hyaluronsäure. Die mit Natriumhyaluronat vermischten cerabone® Granula werden in einem praktischen Blister geliefert, der eine komfortable Hydratation ermöglicht (Abbildung 2). Dank des ausgeprägten Flüssigkeitsbindevermögens von Natriumhyaluronat bildet cerabone® plus nach der Hydratation ein „Sticky-Bone“-Knochenersatzmaterial mit exzellenten Handhabungseigenschaften, das einfach aufgenommen und in den Defektbereich eingebracht werden kann. Da sich cerabone® plus durch eine ausgezeichnete Biokompatibilität und Osteokonduktivität auszeichnet, ist dieses Biomaterial bei chirurgischen Verfahren zur Augmentation des Alveolarkamms ein idealer Ersatz für den patienteneigenen Knochen23,24. Indem dem bovinen Knochenersatzmaterial allogene Knochenpartikel zugefügt werden, wird das regenerierte Gewebe homogener und weniger dicht (postoperative DVT-Aufnahme Abbildung 3D).
2.3. Vorbereitung und Handhabung von cerabone® plus in Kombination mit maxgraft® Granula
cerabone® plus wird in einer sterilen Blisterpackung geliefert. Diese enthält die erforderliche Menge Granula, die für die Alveolarkammaugmentation vor dem Setzen eines Einzelimplantats benötigt wird (Abbildung 2). Im ersten Schritt werden die spongiösen maxgraft® Granula, ein Allograftmaterial (botiss biomaterials GmbH, Zossen, Deutschland), welches die Neubildung von Knochengewebe und einen schnellen Umbau in patienteneigenen Knochen nachweislich fördert, mit cerabone® plus vermischt, um eine zusammenhängendere Masse zu erhalten. Anschliessend wird das Xenograft-Allograft-Gemisch direkt im cerabone® plus Blister mit steriler Kochsalzlösung hydratisiert. Da das in cerabone® plus enthaltene Natriumhyaluronat ein hohes Flüssigkeitsbindevermögen hat, wird für die Hydratation nur sehr wenig Flüssigkeit benötigt. Durch sorgfältiges Vermischen der Flüssigkeit mit dem Biomaterialiengemisch entsteht ein gebrauchsfertiges „Sticky-Bone“-Knochenersatzmaterial. Während intraossäre Defekte möglicherweise von einem höheren Anteil an Allograften profitieren, könnte sich bei der Füllung von Defekten an den äusseren Flächen oder Defekten in der ästhetischen Zone ein höherer Anteil des resorptionsstabilen Knochenersatzmaterials cerabone® von Vorteil erweisen. Je mehr maxgraft® Granula beigemischt werden, desto fester wird die Konsistenz des Materials. Im Ergebnis erhält man eine zusammenhängende, hervorragend formbare Masse im Sinne eines „Sticky-Bone“-Materials, das sich einfach in den Defekt modellieren lässt.
2.4. Chirurgisches Verfahren
Die präoperativen klinischen Untersuchungen, das gesamte chirurgische Verfahren und die postoperative Versorgung wurden wie in unseren früheren Arbeiten zur Alveolarkammaugmentation beschrieben durchgeführt1,4,5.
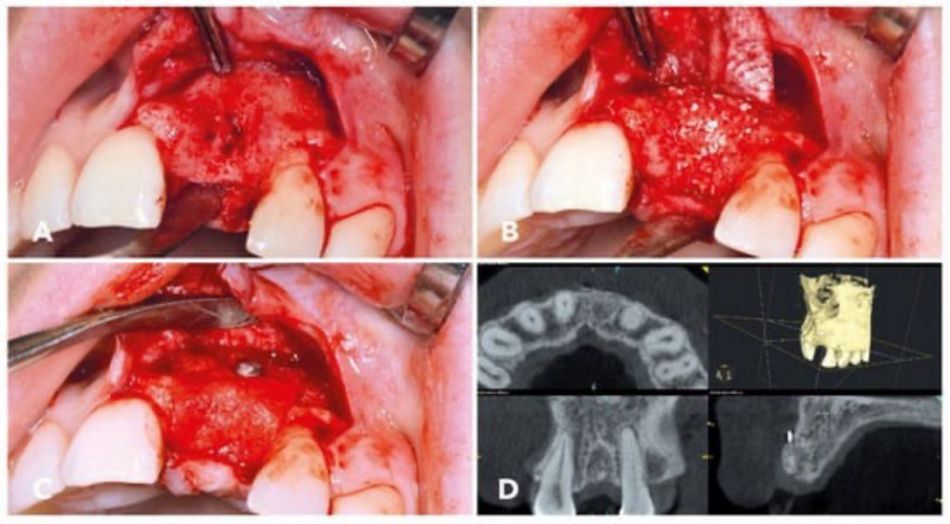
Nach der Lappenpräparation war ein Knochendefekt der Klasse II zu erkennen (Abbildung 3A). Die intraossäre Defektkavität wies unregelmässige Konturen auf. Der Defekt wurde unter Verwendung eines klebrigen Xenograft-Allograft-Gemisches (cerabone® plus in Kombination mit maxgraft® Granula) rekonstruiert. Die Konturen des umliegenden intakten Alveolarknochens wurden bei der Rekonstruktion sorgfältig berücksichtigt. Abbildung 3B zeigt die klinische Situation, nachdem das klebrige Xenograft-Allograft-Material in den Defektbereich eingebracht wurde. Das Xenograft-Allograft-Gemisch wirkte kompakt und fest mit dem darunter liegenden Knochen verbunden. Um den Augmentationsbereich zu schützen, wurde eine Barrieremembran aus porcinem Perikardium mit einem langsamen Resorptionsprofil platziert (Jason® membrane, botiss biomaterials GmbH, Zossen, Deutschland). Die Membran wurde bukkal mit einem Titanstift am Knochen fixiert und palatinal unter das Periost geschoben. Abbildung 3C zeigt die über dem Augmentationsbereich platzierte und fixierte Kollagenmembran.
Vier Monate nach dem Augmentationsverfahren wurde eine DVT-Aufnahme angefertigt (Abbildung 3D). Die Aufnahme zeigte bereits eine partielle Defektregeneration mit einem insbesondere im krestalen Bereich rekonstruierten und volumenstabilen bukkalen Knochenvolumen.
Die routinemässige postoperative Versorgung beinhaltete die Gabe von Amoxicillin und Clavulansäure (625 mg, oral, drei Mal täglich über vier Tage), Ibuprofen (600 mg, oral, alle sechs Stunden nach Bedarf) und Mundspülungen (Chlorhexidinlösung 0,2 %, drei Mal täglich über sieben Tage). Über einen Zeitraum von sechs Monaten postoperativ wurde die Patientin monatlich einbestellt, um mögliche Komplikationen wie eine Infektion, Schmerzen, Beschwerden, exponiertes Transplantatmaterial oder eine Implantatbeweglichkeit frühzeitig zu erkennen.
2.5. Implantatchirurgisches Verfahren
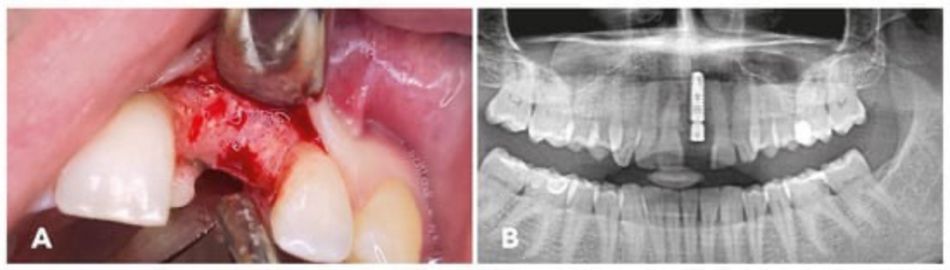
Sechs Monate postoperativ erfolgte das Re-Entry (Abbildung 4A) für das implantatchirurgische Verfahren. Der blutende Knochen deutete auf einen zufriedenstellenden Umbau in patienteneigenen Knochen und eine gute Blutversorgung des Transplantatmaterials hin. Das Implantat wurde wie in einer früheren Arbeit beschrieben gesetzt1. Im ersten Schritt wurde der Fixationspin der Membran entfernt und die Stabilität des Transplantats beurteilt. Das Knochenersatzmaterial erwies sich als gut integriert. Das erreichte Knochenvolumen war zufriedenstellend und hinreichend für eine stabile Implantation. In Regio 21 wurde ein Titanimplantat gesetzt (Medentika; Straumann Group, Basel, Schweiz). Abbildung 4B zeigt den stabilen Sitz des Implantats in Regio 21. Drei Monate nach dem implantatchirurgischen Verfahren wurde das geschlossen eingeheilte Implantat freigelegt und die Patientin erhielt eine verschraubte Krone.
3. Ergebnisse
Während der Heilungsphase im Anschluss an das Augmentationsverfahren traten keine Zeichen für eine Infektion, Wunddehiszenz, exponiertes Transplantatmaterial oder andere postoperative Komplikationen auf. Zum Zeitpunkt des implantatchirurgischen Verfahrens war das Xenograft-Allograft-Gemisch gut im Kieferknochen integriert und das ehemals unzureichende Knochenvolumen war hinreichend wiederhergestellt. Bei den Follow-up-Untersuchungen wurde eine stabile Verankerung des Implantats festgestellt.
An den sechs Messpunkten rund um das Implantat traten keine Sondierungsblutungen auf. Es gab keine Zeichen für eine Mukositis oder Periimplantitis.
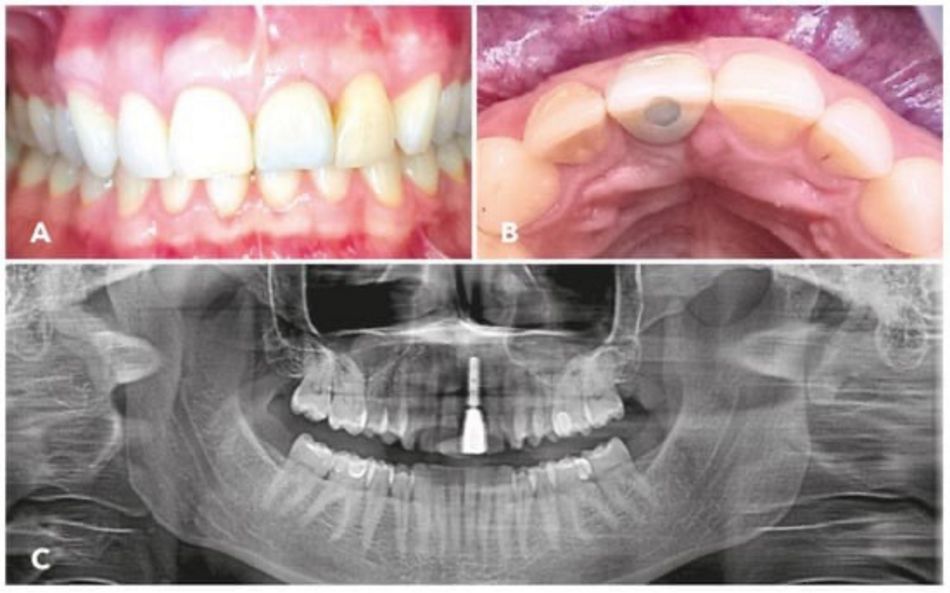
Die Abbildungen 5A und B zeigen die klinische Situation 12 Monate nach Eingliederung der definitiven Krone.
Drei Jahre postoperativ zeigte sich eine stabile Weichgewebesituation ohne Zeichen für eine periimplantäre Mukositis. Die Panorama-Röntgenaufnahme, die drei Jahre nach dem Augmentationsverfahren angefertigt wurde (Abbildung 5C), belegt die exzellente Osseointegration des Implantats. Rund um das Implantat waren keine Zeichen für einen Knochenverlust zu erkennen.
4. Diskussion
cerabone® plus markiert einen signifikanten Fortschritt auf dem Gebiet der Knochenersatzmaterialien, besitzt ein bemerkenswertes regeneratives Potenzial sowie hervorragende angiogene Eigenschaften und eine exzellente mechanische Stabilität. Mit cerabone® plus steht eine vielseitige und zuverlässige Option für ein breites Anwendungsspektrum in der Mundchirurgie zur Verfügung 23,24,27,28,29,30,31. Dank des ausgeprägten Flüssigkeitsbindevermögens von Natriumhyaluronat bildet cerabone® plus nach der Hydratation eine zusammenhängende Masse, die im Vergleich zu herkömmlichen granulären Knochenersatzmaterialien eine effiziente Defektaugmentation, eine präzise Applikation der Partikel und eine schnelle Defektkonturierung ermöglicht.
Alveolarkammaugmentation
Die Alveolarkammaugmentation ist ein wichtiges zahnmedizinisches Verfahren prae implantionem, dessen Ziel es ist, die Struktur des Kieferknochens zu verbessern, um eine solide knöcherne Abstützung der geplanten Dentalimplantate sicherzustellen37,38. Wenn ein Zahn verloren geht oder extrahiert wird, kommt es zu einem Abbau des umliegenden Alveolarknochens und in der Folge zu einer Reduktion des Knochenvolumens und der Knochendichte39,40,41. Ohne eine hinreichende knöcherne Abstützung ist eine zufriedenstellende Osseointegration der Zahnimplantate häufig nicht möglich, sodass Ästhetik und Funktion beeinträchtigt sind42,43. Eine Alveolarkammaugmentation beinhaltet das Einbringen von Knochentransplantat oder Knochenersatzmaterial in den betroffenen Bereich, um die Neubildung von Knochengewebe zu stimulieren oder eine hinreichende Abstützung der Dentalimplantate sicherzustellen38. Autologe Mikrografts sind nachweislich sicher in der Anwendung und führen zu vorhersagbaren Ergebnissen44. Unter den zahlreichen verfügbaren Materialien spielen allogene und xenogene Knochenersatzmaterialien dank ihrer einzigartigen Vorteile eine wichtige Rolle6,45.
Allogene Knochenersatzmaterialien werden aus Knochen menschlicher Spender gewonnen46. Allograft-Materialien wie gefriergetrocknete, demineralisierte Knochen-Allografts oder mineralisierte prozessierte und entzellularisierte Knochen-Allografts werden nach strikten Standards verarbeitet und sterilisiert, um maximale Sicherheit zu gewährleisten und mögliche Immunreaktionen auf ein Minimum zu reduzieren47. Allogene Knochenersatzmaterialien sind unbegrenzt verfügbar und damit eine praktische Option für die Zahnchirurgie48. Ausserdem besitzen sie osteokonduktive Eigenschaften, d. h. sie formen ein Gerüst für die Neubildung von vitalem Knochengewebe und begünstigen eine schnelle und natürliche Knochenregeneration49,50. In mehreren Studien, die die horizontale Alveolarkammaugmentation mit allogenen versus autogenen Knochenblöcken untersuchten, wurden keine Unterschiede bezogen auf die Parameter Implantaterfolg, Knochenresorption und postoperative Komplikationsraten festgestellt1,4,51.
Xenogene Knochenersatzmaterialien werden aus Geweben tierischen Ursprungs gewonnen, gewöhnlich aus bovinen oder porcinen Geweben45,52,53. Wie die allogenen Materialien werden sie prozessiert und gereinigt, um das Risiko für Krankheitsübertragungen und Immunreaktionen zu minimieren7,54. Xenogene Knochenersatzmaterialien besitzen ebenfalls exzellente osteokonduktive Eigenschaften und finden breite Anwendung bei implantatchirurgischen Verfahren7,9,10,11,12,13,18,19. Darüber hinaus bieten bovine Knochenersatzmaterialien wie cerabone®, die in Hochtemperaturverfahren hergestellt werden, dank ihres langsamen Resorptionsprofils Langzeitvolumenstabilität11.
4.2. Verbesserte Knochenregeneration
Das regenerative Potenzial von cerabone® plus und seine Fähigkeit, die Neubildung von Knochengewebe zu unterstützen, wurde übereinstimmend in mehreren Studien aufgezeigt23,24,27,28,29,30,31. cerabone® plus demonstrierte eine exzellente Osteokonduktivität und Biokompatibilität, Eigenschaften, die die Neubildung von robustem Knochengewebe und die Integration in das Empfängergewebe fördern24. Eine Studie kam zu dem Schluss, dass cerabone® plus in verschiedenen klinischen Situationen als eine gute Alternative zu autogenen Knochentransplantaten eingesetzt werden könne24. Zwei voneinander unabhängige histomorphometrische Studien an Wistar-Ratten, Pröhl et al. (2021) und Alkildani et al. (2023), zeigten auf, dass cerabone® plus eine exzellente Biokompatibilität und exzellente osteokonduktive Eigenschaften besitzt28,29.
4.3. Förderung der Angiogenese
In der Knochenregeneration spielt die Angiogenese eine kritische Rolle, da sie das Einspriessen von neuen Blutgefässen, die für die Nährstoffversorgung und den Abtransport von Abbauprodukten erforderlich sind, begünstigt. In dieser Hinsicht zeigt cerabone® plus vielversprechende Ergebnisse. Eine Studie von Kyyak et al. (2022) berichtete, dass cerabone® plus die Angiogenese aktiv unterstützt und auf diese Weise die Entwicklung von gut durchblutetem Knochengewebe fördert23. Diese Ergebnisse unterstreichen das Potenzial von cerabone® plus, den Heilungsprozess zu fördern und zu verbesserten Patientenergebnissen beizutragen.
4.4. Verbesserte mechanische Eigenschaften
Neben den beschriebenen regenerativen Eigenschaften zeigt cerabone® plus auch verbesserte mechanische Eigenschaften und ist damit auch für lasttragende Anwendungen geeignet. Eine Studie von Rakasevic et al. (2023) zeigte auf, dass cerabone® plus eine vorteilhafte Druckfestigkeit und ein günstiges Elastizitätsmodul besitzt und damit geeignet ist, von Periimplantitis betroffene Implantate zu stabilisieren und strukturell abzustützen30. Diese Eigenschaft ist insbesondere bei chirurgischen Verfahren zur Rekonstruktion des Alveolarkamms von Bedeutung, da das Knochenersatzmaterial mechanischen Belastungen standhalten muss, um den langfristigen Implantaterfolg zu unterstützen.
Der grundlegende Vorteil von allogenen und xenogenen Knochenersatzmaterialien liegt in ihrer Wirksamkeit, ihrer Biokompatibilität und ihrer Fähigkeit, die Struktur des Alveolarkamms wirksam zu verbessern. Ein Gemisch aus diesen zwei Materialien kombiniert die günstigen Eigenschaften des bovinen Knochenersatzmaterials (Volumenstabilität) und des Allografts (rasche Regeneration)55. Diese Knochenersatzmaterialien sind eine verlässliche Option für implantatchirurgische Verfahren, da sie eine stabile Basis für Dentalimplantate schaffen7,56. Dank ihrer Verfügbarkeit und einfachen Anwendung stellen sie zudem insbesondere für Patient/innen mit eingeschränkter autogener Knochenverfügbarkeit für die Entnahme eines Transplantats eine wertvolle Behandlungsoption dar.
4.5. Vergleich zu vorherigen Studien
Dieser klinische Fallbericht ist der erste Bericht, der die Langzeitergebnisse einer Alveolarkammaugmentation unter Verwendung einer Kombination aus cerabone® plus und maxgraft® Granula dokumentiert. Gleichzeitig beschreibt er detailliert den chirurgischen Ansatz. Bis dato wurde eine Studie veröffentlicht, in der ein Gemisch aus cerabone® und maxgraft® bei einem Patienten mit Implantatversagen in der Vorgeschichte zur Anwendung kam55. Von den Wissenschaftlern wurde jedoch nicht cerabone® plus verwendet.
Seit cerabone® plus 2020 die CE-Zertifizierung erhielt, wurden bereits mehrere Studien zu diesem neuen Knochenersatzmaterial veröffentlicht. Dabei handelt es sich einerseits um Tierstudien, nämlich eine In-vitro-Studie24 und drei In-vivo-Studien [23,28,29], sowie um Humanstudien: eine klinische Studie, in der cerabone® plus erstmals zur Rekonstruktion des Kieferkamms bei Patient/innen mit Periimplantitis eingesetzt wurde [30], und ein klinischer Fall mit Alveolarkammaugmentation31.
Der vorliegende klinische Fallbericht mit einem Nachbeobachtungszeitraum von 3 Jahren ist der erste Bericht, der die klinische Anwendung einer Xenograft-Allograft-Kombination bei der Augmentation des Alveolarkamms beschreibt. Zusätzlich ist dieser Fallbericht besonders interessant, da das bovine Knochenersatzmaterial cerabone® plus mit einem allogenen Knochenersatzmaterial vermischt wurde, während die Produktbeschreibung von cerabone® plus die Kombination mit einem autogenen Knochentransplantat empfiehlt. Somit präsentiert dieser Fallbericht eine neue und zukunftsweisende Möglichkeit der Anwendung, die den Patient/innen eine Transplantatentnahme erspart.
5. Schlussfolgerungen
Dies ist der erste Fallbericht mit einer Langzeitnachbeobachtung über 3 Jahre, der die erfolgreiche klinische Anwendung eines Xenograft-Allograft-Gemisches (cerabone® plus in Kombination mit maxgraft® Granula) im Rahmen einer Alveolarkammaugmentation prae implantionem dokumentiert. cerabone® plus bietet Volumenstabilität, eine zuverlässige und wirksame strukturelle Abstützung der oralen Weichgewebe im augmentierten Bereich (besonders wichtig in der ästhetischen Zone) und sorgt für den Erhalt des Alveolarkamms. Zusätzlich schützt es in Kombination mit einem allogenen oder autologen Knochentransplantat vor Resorption.