Soluciones regenerativas Straumann® es nuestra contribución para regenerar los tejidos duros y blandos alrededor de los dientes e implantes dentales para mantener una función y estética duraderas. No somos un proveedor más; estamos aquí para ayudarte ofreciéndote soluciones respaldadas científicamente para casos simples y complejos relacionados con la conservación de los dientes, el manejo del lugar del implante y la preservación de los implantes.
Áreas de enfoque
La cartera de un vistazo
Información adicional
Casos clínicos y artículos científicos relacionados con las soluciones regenerativas Straumann® en nuestra revista online.


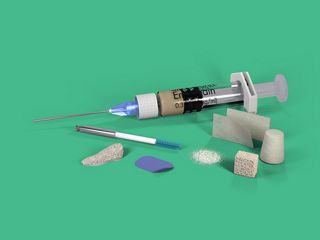
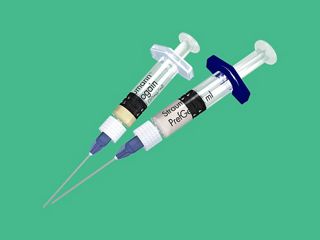
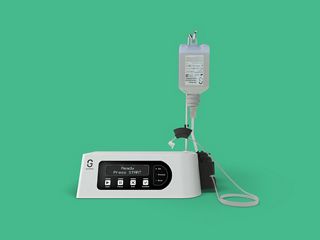
Cartera de productos de soluciones regenerativas Straumann®
Obtén más información sobre nuestra cartera de soluciones regenerativas Straumann®.