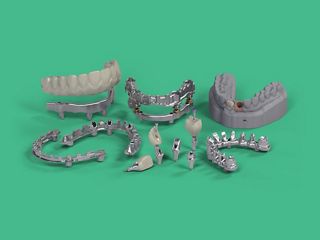
Straumann® crea un ambiente di supporto in cui dentisti e odontotecnici operano in una stretta e proficua collaborazione basata sulla comprensione delle reciproche esigenze e competenze tecniche: le basi per una collaborazione affidabile.
Performance
Assortimento completo di soluzioni protesiche. Sistemi e flussi di lavoro di alta qualità ed efficienti.
Partnership
Soluzioni protesiche progettate con una comprensione dei flussi di lavoro e delle esigenze di dentisti e odontotecnici.
Perfezione
Sistemi originali e compatibili affidabili, clinicamente comprovati. Design preciso e alta qualità costante.